中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (15): 2390-2396.doi: 10.3969/j.issn.2095-4344.2014.15.016
• 组织构建基础实验 basic experiments in tissue construction • 上一篇 下一篇
赤子爱胜蚓核酸酶样蛋白的一级结构特征
于保锋1,2,刘志贞1,2,张悦红1,2,解 军1,2,程牛亮1,2,王建华3,牛 勃1,3
- 山西医科大学,1基础医学院生物化学与分子生物学教研室,2细胞生理学省部共建教育部重点实验室,山西省太原市 030001;3首都儿科研究所生物技术研究室,北京市 100020
Primary structure of nuclease-like proteins from Eisenia foetida
Yu Bao-feng 1, 2, Liu Zhi-zhen 1, 2, Zhang Yue-hong 1, 2, Xie Jun 1, 2, Cheng Niu-liang 1, 2, Wang Jian-hua3, Niu Bo 1, 3
- 1 Department of Biochemistry and Molecular Biology, School of Basic Medical Sciences, Shanxi Medical University, Taiyuan 030001, Shanxi Province, China; 2 Key Laboratory of Cellular Physiology by Shanxi Province and State Ministry of Education, Shanxi Medical University, Taiyuan 030001, Shanxi Province, China; 3 Department of Biotechnology, Capital Institute of Pediatrics, Beijing 100020, China
摘要:
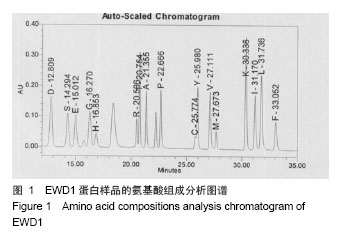
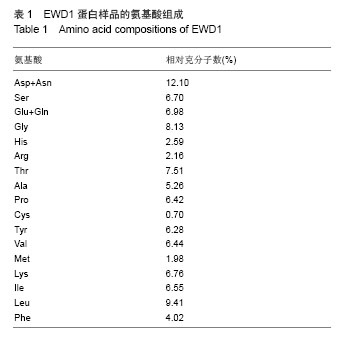
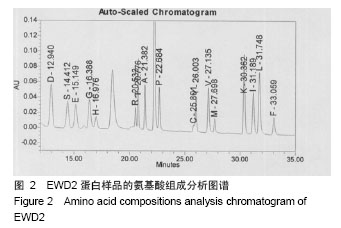
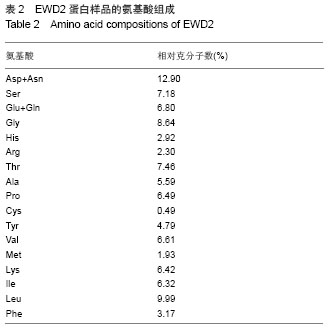
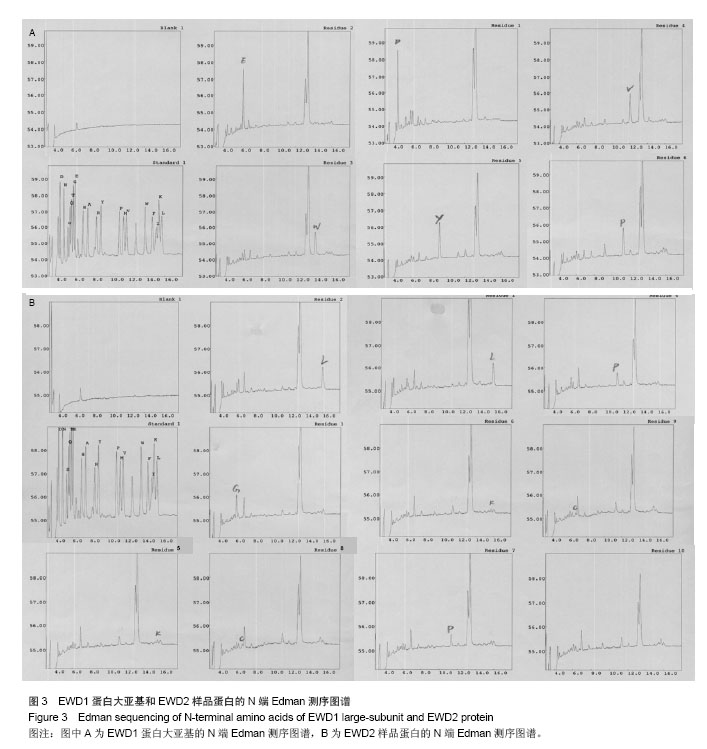
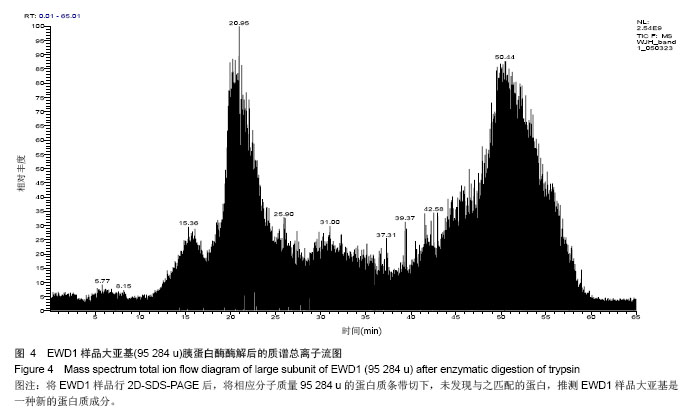
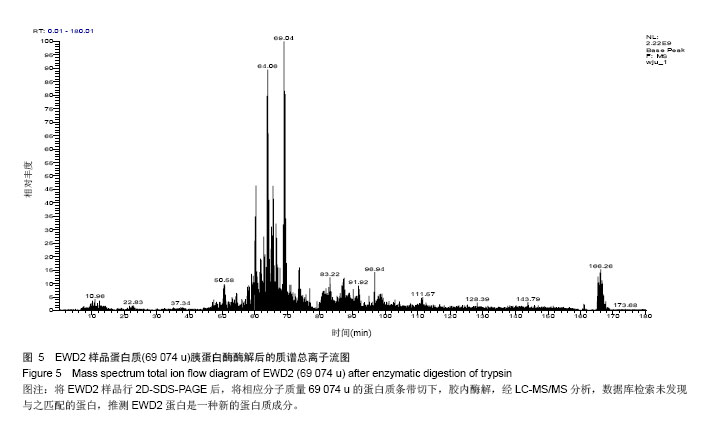
背景:前期研究从赤子爱胜蚓组织中获得一组核酸酶样蛋白,对该组核酸酶样蛋白的一级结构进行研究,有利于揭示其结构的基本性质,为进一步结构与功能的研究奠定基础。 目的:对核酸酶样蛋白EWD1和EWD2进行一级结构的测定。 方法:采用Edman降解法测定EWD1和EWD2的N末端氨基酸序列,采用酸水解法测定其氨基酸组成,LC-MS/MS测定蛋白质内部分氨基酸的序列,MALDI-TOF-MS测定蛋白的含糖量和二硫键数目。 结果与结论:核酸酶样蛋白EWD1和EWD2的氨基酸组成中,天冬氨酸和天冬酰胺之和的含量最高,都达到近10%,疏水氨基酸亮氨酸的含量也较高,半胱氨酸含量较少,氨基酸组成比较显示,该2种酶与其它核酸酶较相似。Edman降解法测定,EWD1蛋白大亚基的N末端6个氨基酸序列为:D、E、W、V、Y、P,EWD2蛋白的N末端9个氨基酸序列为:L、L、G、P、Y、K、P、K、C;串,联质谱的结果提示2种核酸酶为新蛋白;MALDI-TOF-MS法显示1号核酸酶中含有8个半胱氨酸,形成4对二硫键,2号核酸酶中有6个半胱氨酸,形成3对二硫键。EWD1,2均为糖蛋白,EWD1中的含糖量为17.3%,EWD2蛋白中的含糖量为15.6%。
中图分类号:
.jpg)